L’équipe de Sarah Watson, oncologue médicale et chercheuse et les experts en bio-informatique de l’Institut Curie ont mis au point la première méthode efficace, reproductible et utilisable en routine, pour aider à identifier l’origine de cancers jusqu’ici difficiles à soigner.
Les « cancers d’origine inconnue » ou « de primitif inconnu » sont des cancers découverts par la présence de métastases, c’est-à-dire lorsque la maladie s’est propagée à d’autres tissus, sans qu’on ait pu identifier le premier organe touché. Ils représentent entre 2 et 3 % des cas de cancers (soit environ 7 000 patients par an en France) et sont particulièrement difficiles à soigner : d’une part, ils sont diagnostiqués à un stade avancé et, d’autre part, faute de connaître l’origine du cancer, il est impossible de trouver le traitement le mieux adapté.
Jusqu’ici les médecins disposaient de peu de moyens pour déterminer le foyer initial de ces métastases : réaliser un bilan morphologique complet, à l’aide de scanner et PET-scan du corps entier, analyser finement au microscope (anatomopathologie) des échantillons de ces métastases à la recherche d’indices permettant de reconnaître leur origine, et plus récemment, faire appel à la biologie moléculaire pour repérer des mutations, des particularités génétiques typiques de tel ou tel organe. Malgré cela, l’origine tissulaire de ces tumeurs restait inconnue dans un grand nombre de cas, et les patients traités par des approches de chimiothérapie large spectre non spécifiques.
« De nombreuses équipes de recherche s’intéressent à cette question, et plusieurs ont tenté d’identifier des signatures moléculaires de ces tumeurs. » Relève Sarah Watson, oncologue médicale et chercheuse et à l’Institut Curie.
Mais elles utilisent souvent un matériel spécifique, elles sont peu reproductibles et surtout, aucune n’a permis d’augmenter la survie des malades atteints de tels cancers.
L’approche de l’Institut Curie a été différente :
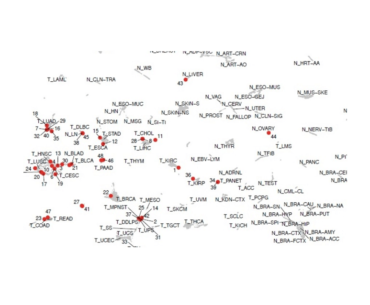
« Plutôt qu’analyser seulement quelques dizaines de gènes, nous avons utilisé la technique de séquençage nouvelle génération RNAseq, qui permet de séquencer tous les gènes exprimés dans une tumeur, afin d’établir un “diagnostic classifier” (classificateur diagnostique) sur la base des profils d’expression de plus de 20 000 tumeurs et tissus normaux. Nous avons mis au point un algorithme de deep learning (apprentissage profond) qui a appris à apparenter avec succès tel ou tel profil ARN à tel ou tel tissu et organe, cancéreux ou non » Détaille Sarah Watson.
Puis, l’équipe de l’Institut Curie a soumis à ce programme informatique les données RNAseq de 48 tumeurs d’origine inconnue. Dans 79 % des cas, l’algorithme a permis d’identifier un tissu d’origine. Chez 11 patients tout juste diagnostiqués, 8 ont pu recevoir un traitement choisi en fonction de ce résultat et tous ont eu un bénéfice du traitement.
Après la publication de cette étude prometteuse dans le Journal of Molecular Diagnostics, l’Institut Curie s’attèle maintenant à faire connaître et appliquer cette méthode dans un plus grand nombre d’établissement de soins grâce à son implication dans la Réunion de concertation pluridisciplinaire nationale consacrée à ces cancers d’origine inconnue et en s’appuyant sur le programme Médecine France génomique 2025, qui prévoit la création de deux premières plateformes génomiques à visée diagnostique et de suivi thérapeutique utilisant le séquençage à très haut débit du génome humain.
Retrouvez la publication originale : https://curie.fr/actualite/publication/linstitut-curie-developpe-un-outil-dintelligence-artificielle-pour